Fedme og relaterede stofskiftesygdomme er blevet globale folkesundhedsproblemer, som er tæt forbundet med forekomsten af hjerte-kar-sygdomme, diabetes og visse kræftformer. Selvom traditionelle behandlingsmetoder som kostkontrol, træningsintervention og lægemiddelbehandling har visse effekter, har de problemer som dårlig compliance, begrænset terapeutisk effekt og betydelige bivirkninger.AOD 9604kapseler et syntetisk 30-aminosyrepolypeptid. Ved at efterligne det væksthormon-frigivende peptidfragment kan det fremme fedtnedbrydning og hæmme fedtophobning og har samtidig potentielle antitumoreffekter. Den store molekylvægt, stærke hydrofilicitet og lette enzymatiske hydrolyse af AOD 9604 resulterer imidlertid i dens lave biotilgængelighed og begrænser dens kliniske anvendelse. Fremkomsten af nanoteknologi har medført revolutionerende ændringer i lægemiddelleveringssystemer. Nanobærere kan opnå målrettet levering, vedvarende frigivelse og forbedret stabilitet af lægemidler ved at regulere partikelstørrelsen, overfladeladningen og modifikationsstrategien for lægemidler. Chitosan, som et naturligt kationisk polysaccharid, har fremragende biokompatibilitet, bionedbrydelighed og lav immunogenicitet. Aminogrupperne på dens molekylære kæde kan binde tæt til negativt ladede cellemembraner eller slimhinder, hvilket øger lægemidlers slimhindegennemtrængelighed. Derudover kan chitosan nanocarriers direkte levere lægemidler til lymfesystemet gennem lymfatisk målretningsteknologi, øge den lokale lægemiddelkoncentration og reducere systemisk toksicitet.
|
|
|





Karakteristika og fremstilling af chitosan nanocarriers
Den kemiske struktur og biologiske egenskaber af chitosan
Chitosan er et naturligt polysaccharid, der produceres ved deacetylering af chitin (hovedsageligt findes i skallerne på rejer og krabber), og dets kemiske struktur er sammensat af -(1,4) -bundet D-glucosamin og N-acetyl-D{{7}. De biologiske egenskaber af chitosan afspejles hovedsageligt i følgende aspekter:
Biokompatibilitet
Chitosan kan nedbrydes in vivo af enzymer såsom lysozym til ikke-toksiske glucosaminmonomerer, hvilket viser fremragende biokompatibilitet.
Biologisk nedbrydelighed
Nedbrydningshastigheden af chitosan kan reguleres ved at regulere dets molekylvægt, grad af deacetylering og miljøforhold.
Mucosal adhæsion
Under sure forhold protoneres aminogrupperne på chitosan-molekylkæden, hvilket giver den positive ladningsegenskaber, hvilket gør den i stand til at binde tæt til den negativt ladede slimhinde og forlænge lægemidlets retentionstid på slimhindeoverfladen.
Antibakteriel egenskab
Den positive ladning af chitosan kan interagere med den negative ladning på bakteriecellemembranen, ødelægge cellemembranens integritet og derved udøve en antibakteriel effekt.
Fremstillingsmetoden for chitosan nanocarriers
Fremstillingsmetoderne for chitosan-nanobærere omfatter hovedsageligt ionisk tværbindingsmetode, kovalent tværbindingsmetode, selv-samlingsmetode og kompositkoagulationsmetode.
Ionkryds-tilknytningsmetode:Ved at bruge multivalente anioner såsom natriumtripolyphosphat (TPP) til elektrostatisk at interagere med aminogrupperne i chitosan, dannes en tre-dimensionel netværksnano-gelstruktur. Denne metode er enkel at betjene, har milde forhold og kræver ikke organiske opløsningsmidler. Det er den mest almindeligt anvendte metode til fremstilling af chitosan nanopartikler.
Kovalent tværbindingsmetode:-Chitosan molekylære kæder er bundet sammen gennem kemiske-krydsbindingsmidler såsom glutaraldehyd og kinesin for at danne stabile nanopartikler. Denne metode kan forbedre stabiliteten af nanopartikler, men den kan introducere giftige tværbindingsmidler.
Selv-samlingsmetode:Ved at drage fordel af de hydrofobe interaktioner eller hydrogenbindinger mellem chitosanmolekyler dannes nanopartikler spontant. Denne metode kræver ikke et tværbindingsmiddel, men stabiliteten af nanopartikler er relativt dårlig.
Komposit koagulationsmetode:Chitosan blandes med polymerer med modsat ladning (såsom natriumalginat), og nanopartikler dannes gennem elektrostatisk interaktion. Denne metode kan regulere overfladeladningen og partikelstørrelsen af nanopartikler.
Modifikationsstrategier for chitosan nanobærere
For yderligere at forbedre målretningen, stabiliteten og biotilgængeligheden af chitosan nanocarriers, vedtager forskere ofte overflademodifikationsstrategier.
Modifikation af polyethylenglycol (PEG).
Introduktion af PEG-kæder på overfladen af chitosan-nanopartikler for at danne usynlige nanopartikler reducerer adsorptionen af plasmaproteiner og forlænger cirkulationstiden i kroppen.
01
Målrettet ligandmodifikation
Ved hjælp af kovalent binding eller fysisk adsorption modificeres målrettede ligander såsom folinsyre, transferrin og antistoffer på overfladen af nanopartikler for at opnå aktiv målretning af specifikke celler eller væv.
02
Kvaternær ammoniummodifikation
Ved at indføre kvaternære ammoniumgrupper øges chitosans positive ladningstæthed, og dets opløselighed og slimhindeadhæsion under neutrale forhold forbedres.
03
Liposom kombination
Chitosan nanopartikler kombineres med liposomer for at danne hybrid nanopartikler, som kombinerer fordelene ved begge og forbedrer indkapslingshastigheden og stabiliteten af lægemidler.
04
Lymfatisk målretningsteknologi og dens anvendelse ved levering af AOD 9604
Lymfesystemets anatomi og fysiologiske funktioner
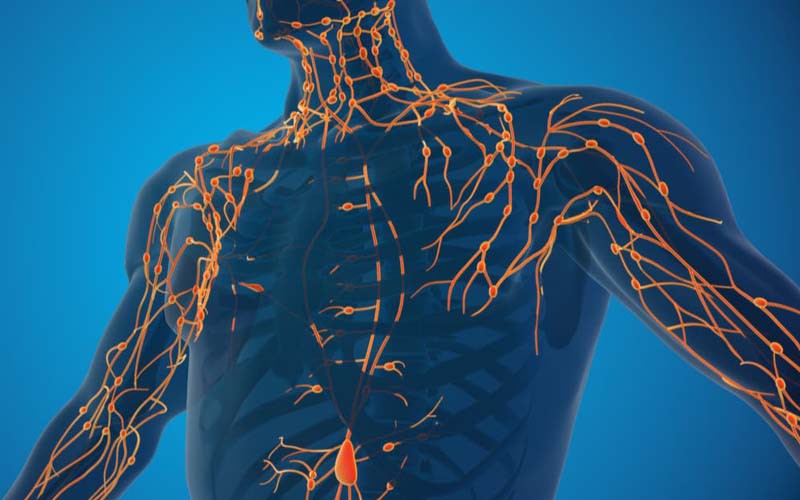
Lymfesystemet er sammensat af lymfekar, lymfeknuder og lymfoide væv, og det er en vigtig kanal til transport af immunceller og præsentation af antigener. Forbindelserne mellem endotelcellerne i lymfekarrene er løsere end dem i kapillærerne, hvilket tillader store molekyler og nanopartikler at passere igennem. Lymfeknuder er vigtige noder i lymfesystemet, rige på immunceller og i stand til at filtrere patogener og tumorceller fra lymfevæske. Tumorceller kan metastasere til regionale lymfeknuder gennem lymfekar og danne metastatiske foci. Inflammatoriske faktorer og metabolitter kan også spredes gennem lymfesystemet, hvilket fører til systemiske læsioner. Derfor kan lægemiddellevering rettet mod lymfesystemet øge den lokale lægemiddelkoncentration betydeligt og blokere sygdommens progression.
Designprincippet for lymfatisk målrettede nanobærere
Designet af lymfatisk målrettede nanobærere skal tage højde for følgende faktorer:
Partikelstørrelse
Forskning viser, at nanopartikler med en partikelstørrelse fra 10 til 100 nm kan trænge ind i lymfesystemet gennem de intercellulære rum i de kapillære lymfekar, mens nanopartikler med en partikelstørrelse større end 200 nm let optages af kapillærer.
Overfladeladning
Negativt ladede nanopartikler optages lettere af lymfekar, mens positivt ladede nanopartikler lettere fjernes af lever og milt.
Overflademodifikation
Ved at modificere de målrettede ligander eller lipofile grupper kan interaktionen mellem nanopartikler og lymfatiske endotelceller forbedres, hvorved den lymfatiske målretningseffektivitet forbedres.
Anvendelsen af chitosan nanocarriers i lymfatisk målretning
Chitosan nanocarriers kan med deres positive ladningsegenskaber og slimhindeadhæsion opnå lymfatisk målretning gennem forskellige lægemiddelleveringsruter.
Oral administration:Chitosan nanopartikler kan transporteres til mesenteriske lymfeknuder via Pyells aggregering (PP). PP er en vigtig bestanddel af intestinalt-associeret lymfoidt væv, rigt på M-celler, som kan optage nanopartikler og transportere dem til lymfeknuder.
Subkutan injektion:De chitosan nanopartikler, der injiceres subkutant, kan absorberes gennem de kapillære lymfekar og trænge ind i de regionale lymfeknuder. Undersøgelser har vist, at retentionstiden for chitosan-nanopartikler i lymfesystemet er væsentlig længere end traditionelle præparater, hvilket muliggør kontinuerlig frigivelse af lægemidler.
Intraperitoneal injektion:Chitosan nanopartikler, der injiceres intraperitonealt, kan absorberes gennem de peritoneale lymfekar og trænger ind i de abdominale lymfeknuder. Denne metode er anvendelig til behandling af bughuletumorer.
Ved levering af AOD 9604 kan chitosan nanocarriers direkte levere lægemidlet til lymfeknuderne nær fedtvæv gennem lymfatisk målretningsteknologi, hvilket fremmer fedtnedbrydning og hæmmer fedtophobning. Desuden kan nanobærere også regulere frigivelseshastigheden af AOD 9604 for at forhindre dets hurtige metabolisme i blodet og forbedre biotilgængeligheden.
Formel design og evaluering
Formuleringsrecept og forberedelsesproces
Dens formuleringsrecept inkluderer chitosan, TPP, AOD 9604 og hjælpestoffer (såsom stabilisatorer, fryse-beskyttelsesmidler osv.). Forberedelsesprocessen anvender ion-krydsbindingsmetoden-. De specifikke trin er som følger:
Fremstilling af chitosanopløsning
Opløs chitosan i 1 % (v/v) eddikesyreopløsning, omrør, indtil det er fuldstændig opløst for at danne en ensartet opløsning.
Opløsning af AOD 9604
Opløs AOD 9604 i deioniseret vand for at danne en stamopløsning.
Fremstilling af nanopartikler
Tilsæt langsomt AOD 9604-stamopløsningen til chitosanopløsningen og omrør for at blande jævnt. Efterfølgende blev TPP-opløsningen droppet i, og nanopartikler blev dannet gennem elektrostatisk-krydsbinding.
Efter-behandling
Centrifuger nanopartikelopløsningen, kassér supernatanten, vask bundfaldet med deioniseret vand, og gentag denne proces tre gange. Til sidst blev nanopartiklerne fryse-tørret for at opnå AOD 9604 Capsule.
Formuleringskarakterisering og kvalitetsevaluering
Partikelstørrelse og Zeta-potentiale
Partikelstørrelsen og Zeta-potentialet for nanopartikler blev bestemt ved dynamisk lysspredning (DLS). Resultaterne viser, at partikelstørrelsen af AOD 9604-kapslen er 80-120 nm, og Zeta-potentialet er +20-+30 mV, hvilket indikerer, at den har god dispergerbarhed og stabilitet.

Morfologisk observation
Nanopartiklernes morfologi blev observeret ved transmissionselektronmikroskopi (TEM). Resultaterne viser, at kapslen har en regulær sfærisk form, med en glat overflade og intet tydeligt agglomerationsfænomen.

Lægemiddelpåfyldning og indkapslingseffektivitet
Lægemiddelbelastningen og indkapslingseffektiviteten af nanopartikler blev bestemt ved højtydende væskekromatografi (HPLC). Resultaterne viser, at lægemiddelbelastningen af kapslen er 15-20%, og indkapslingshastigheden er 80-90%.

In vitro frigivelseseksperiment
Nanopartiklerne blev anbragt i den simulerede lymfevæske (pH 7,4, indeholdende 0,1% Tween 80), og frigivelsesadfærden af AOD 9604 blev bestemt ved dialyse. Resultaterne viser, at frigivelseshastigheden af denne kapsel i den simulerede lymfevæske er betydeligt langsommere end frigivelseshastigheden for det frie lægemiddel, og den har vedvarende-frigivelseskarakteristika.

Farmakodynamik og sikkerhedsevaluering

Fede musemodeller
Overvægtige mus induceret af en kost med højt-fedtindhold blev tilfældigt opdelt i 4 grupper: kontrolgruppen, den frie AOD 9604-gruppe, den tomme nanopartikelgruppe og kapselgruppen. Efter kontinuerlig administration i 4 uger blev legemsvægt, kropsfedtprocent, blodlipidniveau og inflammatorisk faktorniveau for mus bestemt. Resultaterne viste, at kropsvægten og kropsfedtprocenten af mus i denne kapselgruppe var signifikant reduceret, og blodlipidniveauerne og inflammatoriske faktorniveauer var også signifikant lavere end dem i den frie AOD 9604-gruppe, hvilket indikerer, at det har en signifikant effekt på vægttab og forbedring af metabolisk syndrom.
Tumor lymfatisk metastasemodel
Musebrystcancerceller blev inokuleret i trædepuderne på mus for at etablere en tumorlymfatisk metastasemodel. Musene blev tilfældigt opdelt i to grupper: kontrolgruppen og kapselgruppen. Efter kontinuerlig administration i 2 uger blev tumormetastasen af popliteale lymfeknuder i mus observeret. Resultaterne viste, at antallet af lymfeknudemetastasefoci i kapselgruppen af mus var signifikant mindre end i kontrolgruppen, hvilket indikerer, at det har den virkning at hæmme lymfeknudemetastase af tumorer.


Sikkerhedsvurdering
Sikkerheden af produktet blev evalueret ved at måle lever- og nyrefunktionsindikatorer (ALT, AST, BUN, Cr) hos mus og udføre histopatologisk undersøgelse. Resultaterne viste, at det ikke havde nogen signifikant effekt på lever- og nyrefunktioner hos mus. Der blev ikke fundet tydelige abnormiteter ved den histopatologiske undersøgelse, og sikkerheden var forholdsvis god.
Kliniske anvendelsesmuligheder og udfordringer
Udsigter til klinisk anvendelse
AOD 9604 Capsule har med dens lymfatiske målretningsegenskaber og vedvarende-frigivelseseffekt brede anvendelsesmuligheder i behandlingen af fedme, metabolisk syndrom og tumor-relaterede lymfatiske metastaser.
Fedme behandling
Nanopartikler kan fremme fedtnedbrydning og hæmme fedtophobning ved at målrette lymfeknuder i nærheden af fedtvæv, hvilket giver nye behandlingsmuligheder for overvægtige patienter.
Metabolisk syndrom behandling
Nanopartikler kan forbedre stofskiftesygdomme såsom dyslipidæmi og insulinresistens og reducere risikoen for hjerte-kar-sygdomme og diabetes.
Tumor lymfatisk metastasebehandling
Nanopartikler kan målrette mod tumor-drænende lymfeknuder for at blokere tumorcellers lymfatiske metastaser og forbedre overlevelsesraten for tumorpatienter.
Tekniske udfordringer og løsninger
Selvom chitosan nanocarriers har vist betydelige fordele i lægemiddellevering, står deres kliniske anvendelse stadig over for mange udfordringer.
Opløseligheden af chitosan
Opløseligheden af chitosan påvirkes væsentligt af pH, hvilket begrænser dets anvendelse under neutrale eller alkaliske forhold. Løsningerne omfatter kvaternær ammoniummodifikation, indførelse af hydrofile grupper eller indførelse af kompositbærersystemer.
Stor-produktion af nanopartikler
I øjeblikket udføres fremstillingen af nanopartikler for det meste i laboratorieskala, hvilket gør det vanskeligt at opnå industriel produktion. Løsningerne omfatter optimering af forberedelsesprocessen, udvikling af kontinuerligt produktionsudstyr og etablering af strenge kvalitetskontrolstandarder.


Nanopartiklers in vivo skæbne
Nanopartiklernes absorptions-, distributions-, metabolisme- og udskillelsesprocesser (ADME) i kroppen er komplekse og kræver-dybdegående undersøgelse af deres in vivo-adfærd. Løsningerne omfatter brugen af teknikker såsom radioaktiv isotopmærkning og fluorescensbilleddannelse til at spore in vivo-fordelingen af nanopartikler.
Sikkerheds- og effektivitetsevaluering
Den langsigtede-sikkerhed og effektivitet af nanopartikler skal verificeres gennem store-kliniske forsøg. Løsningerne omfatter styrkelse af præklinisk forskning, optimering af design af kliniske forsøg og etablering af et komplet bivirkningsovervågningssystem.
Konklusion
Denne artikel tager chitosan nanocarriers som kernen og kombinerer lymfatisk målretningsteknologi for systematisk at udforske dens innovative anvendelse i AOD 9604 kapselpræparater. Undersøgelser har vist, at chitosan nanocarriers kan opnå lymfatisk målrettet levering af AOD 9604 ved at regulere partikelstørrelse, overfladeladning og modifikationsstrategier, hvilket væsentligt forbedrer lægemidlets biotilgængelighed og effektivitet. Denne kapsel viser brede anvendelsesmuligheder i behandlingen af fedme, metabolisk syndrom og tumor-relaterede lymfatiske metastaser. Tekniske udfordringer såsom chitosanopløselighed, stor-produktion af nanopartikler, in vivo skæbne og evaluering af sikkerhed og effektivitet mangler dog stadig at blive behandlet. I fremtiden, med den fortsatte udvikling af nanoteknologi og uddybningen af klinisk forskning, forventes det at blive en ny mulighed for behandling af relaterede sygdomme og yde væsentlige bidrag til årsagen til menneskers sundhed.
AOD 9604-kapsler repræsenterer et gennembrud inden for fedmeterapi og tilbyder en målrettet tilgang til fedtstofskiftet uden faldgruberne ved traditionelle hGH- eller appetitundertrykkende stoffer. Dens dobbelte virkning på lipolyse og lipogenese, kombineret med en fremragende sikkerhedsprofil, placerer den som en hjørnesten i fremtidige vægtstyringsregimer. Mens regulatoriske hindringer fortsætter, lover igangværende forskning og formuleringsforbedring at udvide dets kliniske anvendelser. Mens verden kæmper med fedmekrisen, står AOD 9604 som et vidnesbyrd om bioteknologiens magt til at omdefinere sundhedsresultater.
Populære tags: aod 9604 kapsel, leverandører, producenter, fabrik, engros, køb, pris, bulk, til salg









