Natriumbromat(NaBrO3) (sammenkæde:https://www.bloomtechz.com/synthetic-chemical/sodium-bromate-powder-cas-7789-38-0.html) er et farveløst krystallinsk, hvid partikel eller krystallinsk pulver uden lugt. Nedbrydes og frigiv ilt ved 381 grader. Opløselig i vand, uopløselig i ethanol, og den vandige opløsning er neutral. Det har god opløselighed i vand og kan hurtigt opløses og producere protonudvekslingsreaktioner. Dens opløselighed stiger med stigende temperatur. Det er oxiderende og kan forårsage forbrænding eller eksplosion ved friktion med organiske forbindelser, sulfider og let oxiderende stoffer. Irriterende. Det er relativt stabilt ved stuetemperatur, men nedbrydningsreaktioner forekommer ved høje temperaturer eller under opvarmningsbetingelser, hvilket genererer natriumchlorid og oxygen. Den termiske ledningsevne er lav, hvilket gør den til en dårlig varmeleder. Det har god transmittans til ultraviolet og synligt lys, så det kan bruges som et optisk materiale. Kemiske reagenser til fremstilling af uorganiske kemiske produkter og bestemmelse af phenoler; Almindeligvis brugt som en oxidant, laboratorie brom generator, kosmetisk kold perm agent; Anvendes industrielt som uldefterbehandlingsmiddel samt til udvinding og rensning af ædel- og tungmetaller; Anvendes til volumetrisk analyse og kan også bruges som oxidationsmiddel; Anvendes til volumetrisk analyse og også som oxidationsmiddel; Udskrivnings- og farvningshjælpemidler, daglige kemikalier såsom permanente midler, kemiske reagenser og rengøringsmidler.
Den molekylære strukturanalyse af natriumbromat er en detaljeret undersøgelse og beskrivelse af stoffets struktur og sammensætning. Det omfatter analyse af typer, mængder, forbindelsesmåder og rumlige arrangement af atomer i molekyler.
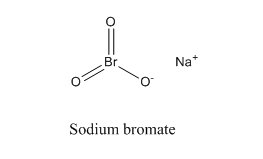
1. Molekylformel og kemisk formel:
Den molekylære formel for natriumbromat er NaBrO3, som indeholder tre elementer: natrium (Na), brom (Br) og oxygen (O). Den kemiske formel kan afsløre den relative andel af hvert grundstof i forbindelsen.
2. Udvidet og elektronisk struktur:
Den udvidede formel for NaBrO3 kan yderligere demonstrere forbindelsen mellem atomer i molekyler. Na danner en ionbinding med Br, mens Br danner en kovalent binding med O. På grund af sin høje elektronaffinitet og elektronegativitet vil oxygen danne kovalente bindinger med to bromatomer. Samlet set indeholder natriumbromatmolekylet én Na+-ion og én BrO3--ion.
3. Krystalstruktur:
Et enkelt natriumbromatmolekyle er sammensat af positive og negative ioner. I krystalstrukturen er disse ioner forbundet med hinanden gennem ionbindinger og danner en krystalstruktur i et specifikt arrangement. Normalt danner NaBrO3 en sekskantet krystalstruktur.
4. Molekylær geometri:
Den geometriske struktur af et natriumbromatmolekyle kan beskrives ved bindingsvinklen mellem atomer i molekylet. I BrO3-ionen danner bromatomet (Br) en trekantet keglestruktur med det centrale oxygenatom (O). Afstanden mellem bromatomet og det centrale oxygenatom er længere end de to andre oxygenatomer.
5. Molekylære egenskaber:
Natriumbromat har nogle særlige molekylære egenskaber. Det er et farveløst, lugtfrit fast stof, der kan opløses i vand. Denne forbindelse har oxiderende egenskaber og kan nedbrydes for at producere ilt under termiske forhold.
Den moderne navngivning af natriumbromat begyndte i slutningen af det 19. til begyndelsen af det 20. århundrede, da videnskabsmænd udførte omfattende forskning i forbindelser, der indeholder bromelementer.
I de tidlige dage, efter opdagelsen af brom, begyndte kemikere at udforske dets forbindelser. Bromsyre er en almindelig bromforbindelse med den kemiske formel HBrO3, hvor H er brintelementet, Br er bromelementet, og O er iltelementet. Bromsyre har stærke oxiderende egenskaber og er en stærk syre, så forskere er begyndt at studere dens saltforbindelser.
I processen med at studere bromat opdagede forskerne, at natriumbromat er en stærkt oxiderende forbindelse, der kan oxidere andre stoffer under sure forhold. Derfor har natriumbromat været meget brugt inden for områder som oxidanter og blegemidler.
For bedre at kunne beskrive egenskaberne og anvendelserne af natriumbromat begyndte videnskabsmænd at navngive det. I betragtning af at natriumbromat er sammensat af natrium og bromationer, antog de navnet "natriumbromat". Blandt dem repræsenterer "natrium" kationer i saltet, og "bromat" repræsenterer anioner i saltet.
Med tiden blev navnet "natriumbromat" efterhånden bredt accepteret og brugt og blev standardnavnet for denne forbindelse. Selvom natriumbromat også omtales som natriumbromid i noget litteratur, er udtrykket "natriumbromat" mere almindeligt brugt.
Kort sagt kan oprindelsen af navnet "natriumbromat" spores tilbage til det tidlige 20. århundrede, hvor videnskabsmænd begyndte at studere forbindelser af brom og opdagede, at natriumbromat har høj oxidationsresistens og anvendelser. Med tiden blev navnet "natriumbromat" efterhånden bredt accepteret og brugt og blev standardnavnet for denne forbindelse.

Natriumbromat har stærke oxiderende egenskaber og kan deltage i forskellige kemiske reaktioner.
1. Reaktioner med organisk stof:
Natriumbromat kan gennemgå oxidative additionsreaktioner med umættede bindinger (såsom dobbelt- eller tredobbeltbindinger) i organiske forbindelser, hvilket aktiverer organiske molekyler. For eksempel kan natriumbromat oxidere phenol til quinonforbindelser, såvel som fedtsyrer eller ketonforbindelser til - Ketonsyre.
2. Reaktion med reduktionsmiddel:
Natriumbromat kan gennemgå redoxreaktioner med reduktionsmidler såsom mercaptaner og phenoler. For eksempel kan natriumbromat reagere med thiourinstof under alkaliske betingelser for at opnå bromid og svovloxid.
3. Reaktioner med ammoniumforbindelser:
Natriumbromat kan reagere med ammoniumforbindelser såsom ammoniakgas og ammoniumchlorid for at danne ammoniumbromid og hypobromat. For eksempel kan natriumbromat reagere med ammoniak for at opnå ammoniumbromid og hypobromat.
4. Reaktioner med brandfarlige stoffer:
Natriumbromat kan reagere med brændbare stoffer som svovl og fosfor og danne eksplosive blandinger. For eksempel kan natriumbromat reagere med svovl for at opnå natriumsulfat og hypobromat.
5. Kontakt med svovlsyre kan forårsage forbrænding:
Natriumbromat gennemgår kemiske reaktioner i svovlsyre og kan forårsage forbrænding. Derfor bør kontakt med svovlsyre undgås ved brug af natriumbromat.
Sammenfattende gør de stærke oxiderende egenskaber af natriumbromat det muligt for det at deltage i forskellige kemiske reaktioner. Ved brug af natriumbromat skal man være opmærksom på sikkerheden og undgå kontakt med uforenelige stoffer. Samtidig hjælper forståelsen af natriumbromats reaktionsegenskaber til bedre at forstå og anvende dets anvendelser.

